 煤化工废水中的有机污染物,如吡啶、联苯、咔唑等,难于生物降解,毒性大,色度高,其COD值可达2 000~5 000 mg·L-1。煤化工废水的处理,通常可分为预处理、二级生化处理与深度处理。预处理主要包括隔油、气浮等方法,及对酚类及氨氮等物质进行回收处理;二级生化处理多采用“厌氧+多级好氧”流程,水力停留时间极长;深度处理方法主要有混凝法、高级氧化法等。 煤化工废水经二级生化处理后,色度和COD难以达到目前执行的排放标准,需进一步深度处理。高级氧化法是目前煤化工废水深度处理技术中的一种,包括芬顿法,催化臭氧氧化法等。仝明采用芬顿法处理鲁奇炉加压煤气化废水,过氧化氢和COD投加质量比3:1,反应20 min,COD去除率可达90%;万哲希等采用颗粒活性炭催化臭氧氧化法降解焦化 废水,活性炭投加量20 g·L-1,COD去除率提高了20%。 臭氧氧化应用于深度处理,具有无药剂残留、操作简单、不产生氯化消毒副产物的优点,但臭氧的直接氧化,去除溶解性有机碳的能力有限。SONG等的研究表明,投加3 mg·L-1的臭氧,氧化10 min,对地表水紫外吸收(UV254)的去除率可达71%,而对溶解性有机碳的去除率仅为10%。这表明:相当部分的有机物在臭氧的直接氧化过程中,只是转化为其他的有机物,并没有彻底氧化为CO2和H2O。寻找有效的催化剂,促进臭氧产生自由基,形成高级氧化机制,增强臭氧处理难降解有机物能力,是我们近年来研究的重点。 本实验采用的催化剂,原材料取自一型号的钢材,经加工成刨花状,表面清洗后进行化学改性,直至表面成分稳定,改性方法见课题组专利。材料化学改性后比表面积2 900 m2·m-3,空隙率95.5%,有利于多相流体在其内部错流、紊流,促进多相界面的传质和化学反应。 1 材料与方法 1.1 材料 实验所用煤化工生化出水取自某公司焦化厂,处理工艺是“隔油池+气浮反应池+二沉池+混凝沉淀池”,最终生化出水COD值170 mg·L-1,pH值6.9。 1.2 方法 1.2.1 实验装置 臭氧氧化反应装置主要由臭氧发生系统、反应柱和尾气吸收装置构成,如图 1所示。臭氧发生器以内置的空压机为气源,外接干燥筒,通过调节臭氧发生器上的档位控制臭氧投加量,臭氧气体从反应柱底部的二氧化硅曝气头通入反应柱内,并由反应柱底部的多孔布气板加以扩散。反应柱的有效使用容积为2 L,内径8 cm,高70 cm,反应柱内事先填好一定量的催化剂。 
图1 实验装置图 1.2.2 实验过程 实验前臭氧排空,待臭氧发生器电流计示数稳定、产气量一定后实验。取1.8 L废水加入到反应柱中,臭氧流量控制在1 L·min-1,反应过程从中部取样分析。反应后尾气通入KI溶液吸收瓶吸收。实验后,用硫代硫酸钠溶液滴定被臭氧氧化产生的I2,计算尾气中的臭氧量。 1.3 分析项目及方法 臭氧发生器产生量测定采用碘量法。通过控制反应电流调节臭氧产量,选取了3个反应电流,测得臭氧产量如表 1所示。 
表1 臭氧产量 COD测定采用国标法。TOC采用TOC仪(TOC-L CPH CN-200,岛津)测定,测量前水样先经过0.22 μm滤膜过滤,稀释5倍后进行测定,以保护仪器。 催化剂表面微观形貌采用场发射扫描电子显微镜(FE-SEM-4800-1,日本日立)进行观察,冷阴极场发射电子源,加速电压20 kV。物相定性采用X射线衍射仪(D8 Advance,Bruker),铜靶,扫描范围10°~80°,工作电压40 kV,工作电流40 mA。红外分析采用智能傅里叶红外光谱仪(Nicolet 5700,Nicolet),数字化干涉仪,波数精度0.01 cm-1。EPR实验采用电子自旋共振波谱仪(EM Xplus 10/12,Bruker),信噪比S/N≥2 000:1。 全波长扫描采用紫外分光光度计(TU-1810,北京普析),波长扫描范围200~600 nm,扫描模式选择吸光度,扫描间距1 nm,用超纯水做空白校准。UV254参考EPA415.3,可有效表征水中吸收紫外线的不饱和有机物、腐殖质类大分子有机物、含碳碳双键和碳氧双键的芳香族化合物。 2 结果与讨论 2.1 催化剂表征 图 2是催化剂表面改性前后500倍的电镜扫描图像。催化剂材料改性前表面整体呈螺旋状,表面较为平整,有少许杂质和细微裂缝;表面改性后,表面粗糙呈黑色,且有众多疏松孔状结构,增大了催化剂与水、臭氧三相接触的面积,有利于反应的进行。 
图2 铁基催化剂表面改性前后扫描电镜图像(×500) 图 3是催化剂表面改性前后X射线衍射光谱图。催化剂材料表面改性前主要成分是零价铁(PDF:06-0696),在44.7°和65.0°有2个主要的峰,对应于零价铁的(110)和(200);表面改性后,谱图在21.2°、26.3°、33.2°、35.5°、43.3°、57.4°和63.3°有7个主要的峰,分别对应于羟基氧化铁(PDF:29-0713)的(110)、(120)、(130)、(101)、(220)、(231)和(320),说明表面的零价铁基本转化成羟基氧化铁,成为有效的催化成分。 
图3 铁基催化剂表面改性前后X射线衍射光谱图 图 4是表面改性后的催化剂红外分析光谱图。催化剂在3 126.28 cm-1处有较强且宽的吸收峰,为羟基氧化铁中羟基的伸缩振动,而水的吸收波数(3 400 cm-1)附近没有明显的吸收峰,说明催化剂表面结合水含量较少,2 361.52 cm-1处的吸收峰乃是空气中二氧化碳不对称伸缩造成的;同时,催化剂在880.96 cm-1和794.14 cm-1存在吸收峰,为α-FeOOH的典型峰,位于561.02 cm-1处的Fe—O吸收峰(400~650 cm-1)也说明了催化剂里存在铁氧化产物。 
图4 表面改性后的催化剂红外分析光谱图 2.2 催化臭氧氧化影响因素及效果分析 2.2.1 初始pH值 废水初始pH值是影响催化臭氧氧化效果的主要因素之一。废水初始pH值会极大影响臭氧的分解速度、羟基氧化铁表面羟基的电荷形态及有机物在水溶液中的存在形态,从而影响催化臭氧氧化的效果。实验选取了5个不同的pH值,用1 mol·L-1的硝酸和NaOH溶液调节废水pH值,催化剂投加量为200 g·L-1,臭氧投加量为10.7 mg·min-1,研究不同pH值对催化臭氧氧化效果的影响。单独臭氧氧化实验不调节pH值,为原水pH值(6.9)。 由图 5可知,催化臭氧氧化(catalytic ozonation,CO)的COD去除率可以达到(66.2±1.7)%,比单独臭氧氧化(single ozonation,SO)的(47.6±2.6)%提高了近20个百分点;而TOC去除率则可以达到(58.4±2.1)%,比单独臭氧氧化的(28.8±1.9)%提高了近1倍。 
图5 初始pH值对催化臭氧氧化COD和TOC去除率的影响 调节废水pH值,无论是酸性(pH=4,5),还是碱性(pH=9,10),催化臭氧氧化的效果都不如中性(pH=7)的效果好,这可能是因为羟基氧化铁的零电荷点(pHpzc)在中性附近,过酸和过碱都影响了羟基氧化铁表面羟基的电荷形态。需要注意的是:当pH=4时,COD的去除率不如单独氧化的,但TOC的去除率却比单独氧化的高。这是因为单独臭氧氧化很难降解煤化工生化出水中的难降解有机物,从而TOC去除率低;而pH=4时催化臭氧氧化一定程度上降解了这部分难降解有机物,甚至是难以测出COD的有机物,但效果没有中性和碱性条件下的好,依然有一部分降解不完全,反而被检测出COD,从而COD的去除率反而降低。 2.2.2 催化剂投加量 催化剂为催化臭氧氧化提供了活性位点,通过吸附臭氧、水、有机物,提供三相反应界面,从而影响催化臭氧氧化的效果。实验选取了3个不同的催化剂投加量,不调节pH值(中性),臭氧投加量为10.7 mg·min-1,研究催化剂投加量对催化臭氧氧化效果的影响。 由图 6可知,适量增大催化剂的投加量,确实可以提高催化臭氧氧化的效果。但过多的催化剂提供了过多的活性位点,反而降低了单位活性位点上的臭氧和有机物浓度,从而降低了局部的反应速率,使得整体的反应速率并没有显著提高。如200 g·L-1和400 g·L-1的催化剂投加量差距1倍,但效果增幅不明显。 
图6 催化剂投加量对催化臭氧氧化COD和TOC去除率的影响 2.2.3 臭氧投加量 臭氧是有机物降解的直接动力,其投加量直接影响催化臭氧氧化的速率及效果。实验通过调节所用臭氧发生器电流档位改变臭氧投加量,并用碘量法测出臭氧产生量。废水不调节pH值(中性),催化剂投加量为200 g·L-1。 由图 7可知,不通臭氧,单纯通空气时,催化剂对废水只有吸附作用,此时COD和TOC的去除率仅有(8.6±0.3)%和(12.1±0.4)%。增大臭氧投加量对COD和TOC的去除率的提高有限,这可能与臭氧的利用率有关,有效利用的臭氧较少,但增大臭氧投加量,有利于三相界面的传质,反应速率更快,特别是在短时间内效果显著。 
图7 臭氧投加量对催化臭氧氧化COD和TOC去除率的影响 2.2.4 催化臭氧氧化效果分析 全波长扫描可以反映溶液整体对某一波长光的吸收性,适合分析含多种有机物的实际废水。其中,紫外谱图提供的是常见官能团信息。若溶液在220~250 nm波段有强烈吸收,说明该溶液化合物中存在共轭双键(共轭二烯烃、不饱和醛、不饱和酮),否则可能是饱和脂肪烃、脂环烃或其衍生物;化合物在250~290 nm波段有强烈吸收,说明化合物分子中有苯环存在(以UV254为代表);化合物在300 nm以上有强烈吸收,说明分子中有较大的共轭体系(大分子腐殖质,以UV410为代表)。废水不调节pH值(中性),臭氧投加量为10.7 mg·min-1,催化剂投加量为200 g·L-1。具体联系污水宝或参见http://www.dowater.com更多相关技术文档。 由图 8可知,废水在200~300 nm波段有很强的吸收,300 nm以上波段吸收较弱,处理后各波段吸光度都有所下降,表明单独臭氧氧化和催化臭氧氧化对废水有机物都有作用。其中,随着反应的进行,单独臭氧氧化和催化臭氧氧化在220~250 nm波段的吸收都有所增强,说明溶液中共轭双键增多,这很有可能是废水中苯环开环的结果。相对而言,催化臭氧氧化在220~250 nm波段的吸收较单独臭氧氧化的弱,说明催化臭氧氧化对共轭双键的作用比单独臭氧氧化强,处理效果更好,这也是催化臭氧氧化的TOC去除率更高的原因。 
图8 催化臭氧氧化和单独臭氧氧化废水全波长扫描光谱图 由表 2可知,单独臭氧氧化对废水UV254的去除率为72.1%,催化臭氧氧化对废水UV254的去除率为80.7%,催化臭氧氧化的处理效果优于单独臭氧氧化。 
表2 废水UV254变化 2.3 自由基机理验证 2.3.1 直接验证 电子顺磁共振技术从定性和定量方面检测物质原子或分子中所含的不配对电子(例如自由基),可直接验证自由基的存在。实验在小烧杯中进行,往小烧杯内添加200 mL超纯水,20 g铁基催化剂,连续通入10.7 mg·min-1臭氧1 min,迅速取样检测自由基。 如图 9所示,添加铁基催化剂(图 9(b))通臭氧的反应体系检测出了1:2:2:1的4重峰,而没有添加铁基催化剂(图 9(a))通臭氧的反应体系没有明显信号,说明添加铁基催化剂确实可以使臭氧分解产生羟基自由基,从而氧化煤化工生化出水中的难降解有机物。 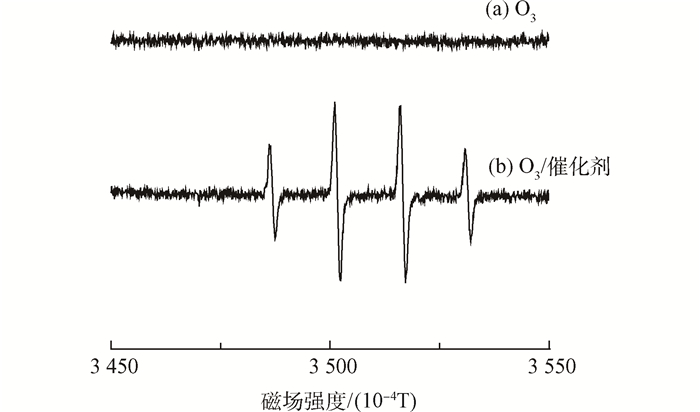
图9 催化臭氧氧化与单独臭氧氧化EPR光谱图 2.3.2 间接验证 为了间接验证催化臭氧氧化过程中有羟基自由基的生成,可向体系添加羟基自由基淬灭剂。实验选择碳酸氢钠,碳酸氢根可以与羟基自由基快速反应(k=1.5×107 L·(mol·s)-1),可作为羟基自由基的淬灭剂。通过向体系添加不同浓度的碳酸氢钠,对比3 h深度处理后的TOC去除率。 如图 10所示,逐渐增加碳酸氢钠的浓度后,单独臭氧氧化的TOC去除率无明显下滑(最多2.4%),而催化臭氧氧化的TOC去除率最多下滑19.2%。添加相同浓度的碳酸氢钠,催化臭氧氧化比单独臭氧氧化的TOC去除率降低得更多,说明催化臭氧氧化过程中产生了更多的羟基自由基,并与有机物反应,去除了更多TOC。 
图10 碳酸氢钠对催化臭氧氧化和单独臭氧氧化废水TOC去除率的影响 3 结论 1) 当pH=7,催化剂投加量为200 g·L-1,臭氧投加量为10.7 mg·min-1时,催化剂效果明显,COD去除率可以达到(66.2±1.7)%,比单独臭氧氧化的(47.6±2.6)%提高了近20个百分点;而TOC去除率则可以达到(58.4±2.1)%,比单独臭氧氧化的(28.8±1.9)%提高了近1倍。 2) 新型铁基催化剂主要成分是羟基氧化铁,催化臭氧氧化的机理是形成羟基自由基氧化的机制,这对彻底氧化有机物意义重大。 3) 催化臭氧氧化与单独臭氧氧化对煤化工生化出水中有机物降解都有作用;对主要存在的带共轭双键的大分子有机物,催化臭氧氧化的效果更为显著。
|